Selvom onkologer i mange tilfælde kan have gode værktøjer og data til at sortere ud og sammenligne forskellige behandlinger, kan nyudviklede terapier undertiden være vanskelige at forudsige, uden klinisk erfaring.
Forskud i viden kommer fra kliniske forsøg, hvor patienter indvilliger i at gå ind i undersøgelser med lægemidler, der har vist et løfte; men som udtrykket "forsøg" betyder, er der altid en vis usikkerhed om, hvor godt et lægemiddel vil udføre, og hvem vil gavne mest – det vil sige, hvilke patienttyper og hvilke undergrupper af kræft.
Hvad er kræftimmunoterapi?
Kræft immunterapi er en behandling, der involverer visse dele af individets immunsystem for at bekæmpe maligniteten. Et eksempel på immunterapi er anvendelsen af monoklonale antistoffer som rituximab og obinutuzumab. Monoklonale antistoffer er menneskeskabte antistoffer eller immunsystemproteiner. Disse antistoffer kan angribe en meget specifik del af en cancercelle i det såkaldte målrettet terapi.
Andre former for cancerimmunterapi omfatter immunkontrolpunkthæmmere, som tager ‘bremser’ ud af immunsystemet for at hjælpe det med at genkende og angribe kræftceller.
Verden af kræftimmunterapi er på ingen måde begrænset til ovenstående eksempler, men nye ideer til at bruge din krops eget immunsystem til bekæmpelse af kræftcellerne fortsætter med at blive udviklet og testet.
virker immunterapi for alle kræftformer?
Hver person er unik, og hver persons kræft er unik; Ikke alle reagerer på samme måde som den samme immunterapi.
Effektivt måling på forhånd, hvilke personer der mest sandsynligt vil reagere på en immunterapi ville være fordelagtige fra flere vinkler. For patienten kunne det spare afgørende tid, hvilket kunne oversætte til klinisk fordel.
Med andre ord vil du ikke spilde din tid eller risiko bivirkninger forsøger noget, der sandsynligvis vil have en minimal effekt, når der kan være en "større pistol" eller mere effektiv terapi til rådighed. Men hvordan kan man på forhånd kende denne type ting? En historie om, hvordan onkologer og kræftforskere går om at gøre dette begynder med noget, der hedder neoantigener.
Neoantigener: Kræftens Achilles Heal?
Kræftceller kan være sneaky. De har ofte en række ændringer i deres gener, hvoraf nogle kan svare til deres evne til at gøre dårlige ting, som normale, sunde celler ikke kan. Nogle af disse ændringer medfører faktisk fysiske forskelle i eller på ydersiden af kræftcellerne, der kan påvises af immunsystemet. Disse dele af kræftceller, som immunsystemet kan genkende som fremmed, kaldes "neoantigener."
Neo, hvilket betyder nyt, fordi de opstår nyligt fra
vores egne celler, er gået af med kræft , i modsætning til de almindelige antigener forskere plejer at tale omkring i smitsomme sygdomme, for eksempel.Regelmæssige antigener kan findes på ydersiden af bakterier eller for virusinficerede celler. I modsætning hertil er neoantigener som røde flag, der kan signalere immunsystemet, som vores egne celler misforstår.
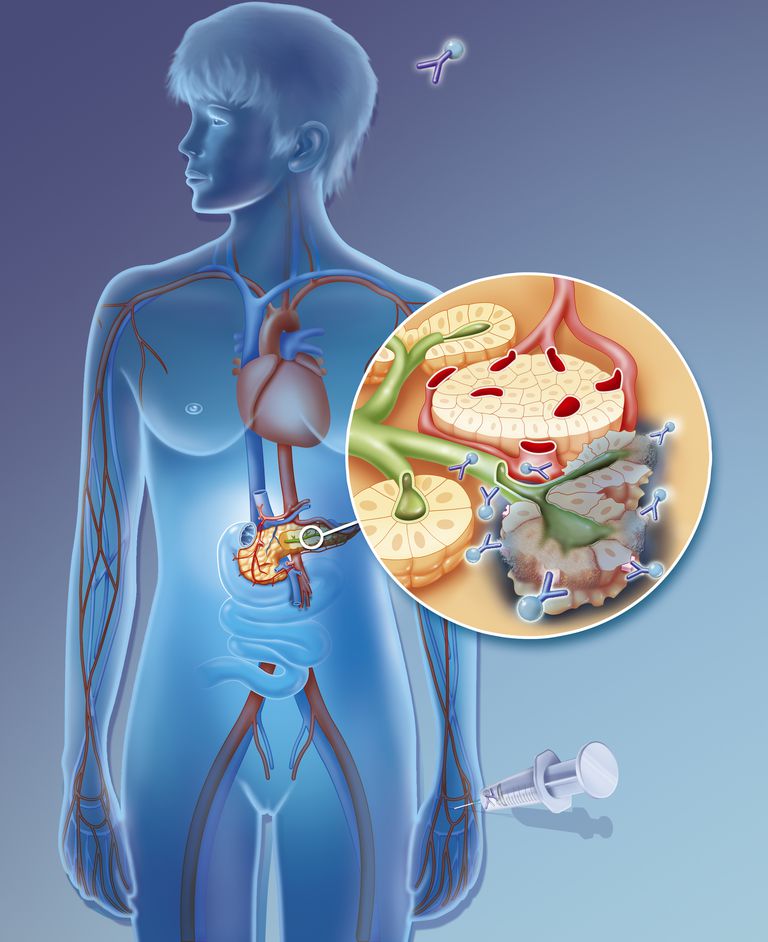
Neoantigener fører til aktiveringen af hvide blodlegemer, der er kendt som T-celler – immunsystemets soldater. Disse soldat-T-celler rejser derefter blodkarrene, ligesom de antikke Romers brostensveje, for at nå frem til de uretfærdige maligne celler, infiltrere tumoren og hjælpe med at decimere lokalbefolkningen af maligne celler.
Så neoantigener er en af nøglerne til immunbaserede anti-cancer-terapier.
Når det er sagt, at vinde kampen sjældent involverer immunterapi alene, og der er normalt behov for en mere forkrydset jordtype. immunoterapi anvendes ofte i forbindelse med cytotoksisk kemoterapi og / eller og andre immunpatienter afhængigt af malignitet og den enkelte patient.
Vil immunterapi virke for mig?
Dette er et vigtigt spørgsmål i moderne onkologi, og en der arbejdes aktivt. I den sammenhæng kan to karakteristika af dine kræftceller hjælpe læger med at forudsige, hvor godt tilgængelige immunterapier vil fungere: TMB og MSI.
Tumor mutationsbelastning eller
TMB kan betragtes som et indeks for alle de ændringer i gener i kræftcellerne, der er gået forkert, for eksempel, der plejede at kode for alle de normale ting en celle måtte have brug for -men der har ændringer eller mutationer i tilfælde af kræftceller. TMB kaldes også undertiden som total mutationsbelastning eller mutationsbelastning.Tumorer, der har høj TMB, antages at have mere neoantigener og kan derfor reagere bedre på immunterapi. Kræftceller kan ende med høj TMB gennem eksponeringer forbundet med kræft, herunder til tobak eller UV-lys. En anden måde er gennem mikrosatellit ustabilitet, eller
MSI , et teknisk udtryk, der refererer til et problem med din krops naturlige mekanismer til DNA-reparation – et problem, der resulterer i stærkt skiftende og inkonsekvente længder af gentagne DNA-gensekvenser.Et firma kaldet Foundation Medicine tilbyder nu de første fuldt integrerede, validerede vurderinger af TMB som en del af FoundationOne-analysen, som kan bidrage til at forudsige en persons potentielle respons på immunterapi.
"Fejlagtige genomer er den fællesnævner for alle kræftformer", forklarer Vincent Miller, MD, cheflærer ved Foundation Medicine. "Tumorer med et særligt stort antal mutationer er mere tilbøjelige til at producere nye, unormale proteiner kaldet neoantigener. Immunsystemet genkender disse neoantigener som fremmed og fortsætter med højvarsling og initierer en kompleks serie af trin til at angribe tumoren. "
Vil en Immun Checkpoint Inhibitor virke for mig?
Grunden tykker i, at nogle kræftformer har udviklet ekstremt snige måder at undvige immunsystemet ved at gøre proteiner, der
inaktiverer visse typer af dine immunceller. En biologisk afskærmningsanordning, hvis du vil. For at forhindre kræft i at kappe sig selv på denne måde, er nogle immunterapier designet til at blokere disse immunsupprimerende proteiner. Disse immunoterapier, kendt som immunkontrolpunktinhibitorer
, indbefatter de betegnede anti-PDl- og anti-PDL1-antistoffer. Og som med andre former for immunterapi er der tegn på, at der foreslås højere niveauer af neoantigener i kræftcellerne, der er forbundet med bedre responser på immune kontrolpunktsinhibitorer. Responsen til kontrolpunkt-hæmmere varierer fra ca. 20 procent i lungekræft til 80 procent i Hodgkin-lymfom. Årsagen til, at visse tumorer reagerer på kontrolpunktsinhibitorer, og andre ikke er uklare.Betydningen af at forudsige klinisk reaktion
Disse prædiktive værktøjer og deres succes var et emne af samtale på dette års møde i American Society of Clinical Oncology, eller ASCO.
TMB har vist sig at forudsige en større sandsynlighed for respons og længere varighed af respons på cancerimmunterapier hos patienter med blærekræft, lungekræft, melanom og andre avancerede kræftformer. Foruden TMB måler FoundationOne også mikrosatellit ustabilitet, der repræsenterer en enkelt test til vejledning af terapeutiske beslutninger for målrettede terapier, kliniske forsøg og FDA-godkendte cancerimmunterapier under anvendelse af en enkelt biopsi. "Cancerimmunoterapier er i spidsen for kræftbehandling, og nye kvantitative tilgange er nødvendige for at forudsige kliniske reaktioner på denne vigtige, men også dyre, klasse af terapier," sagde Dr. Miller.
"Muligheden for at måle flere biomarkører på samme tid, herunder TMB og MSI, er et vigtigt fremskridt inden for kræftimmunterapi, og det er unikt for Foundation Medicine," siger Thomas George, MD, GI oncology programleder, University of Florida. "Foundation Medicines kombination af avancerede sekventeringsplatforme og højspecifikke algoritmer giver mig adgang til alle relevante genomiske biomarkører til mine patienter på én gang og hjælper med at spare både tid og væv."
"Vi blev opmuntret af de resultater, der blev fremlagt hos ASCO, herunder muligheden for at identificere patienter, der er mere tilbøjelige til at drage fordel af kontrolpost inhibitor immunterapi," sagde Dr. Miller. "Vores mål er at give læger og patienter mulighed for at udnytte en bred vifte af relevante, brugbare genomiske oplysninger, og vi er glade for at tilbyde vores særprægede løsning til at estimere TMB og MSI samtidigt og med exceptionel nøjagtighed, understøttet af sofistikerede algoritmer og baseret på kontekstuelle indsigter fra vores vidensbase FoundationCORE. Dette er noget, ingen anden næste generations sekventeringsplatform tilbyder. "
Uafhængigt af FoundationOne og FoundationOne Heme-analyserne tilbyder Foundation Medicine også test af PD-1 og PD-L1 proteinudtryk, der giver sammen med FoundationOne-analyserne en fuld suite af kræft immunterapi analyser for onkologer.
Et ord fra Verywell
Selvom dette bestemt er et lovende område, udvikler videnskaben stadig og forskellige tests bliver stadig undersøgt og valideret. Alle nuværende biomarkører til forudsigelse af klinisk respons til kontrolpunktsinhibitorer er kun undersøgelsesmæssige, og der findes i øjeblikket ingen FDA-godkendte tests, der kan forudsige præcist svaret på kontrol af punktinhibitorer.