Klassificering
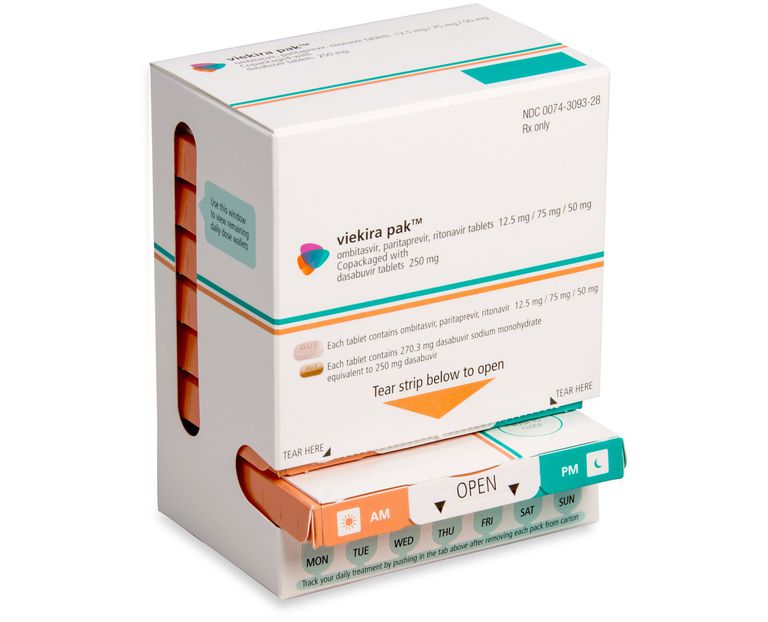
Viekira Pak er en kombinationspakning af lægemiddelkombination, der anvendes til behandling af kronisk hepatitis C (HCV) infektion. Pakken indeholder et kombinationslægemiddel med fast dosis Technivie (ombitasvir + paritaprevir + ritonavir) sammenpakket sammen med lægemidlet dasabuvir.
Lægemiddelkomponenterne ombitasvir, paritaprevir og dasabuvir er direktevirkende antivirale midler (DAA’er), der forstyrrer replikationen af virussen.
Lægemidlet ritonavir, der anvendes hyppigt ved HIV-behandling, er inkluderet for at øge paritaprevirs lægemiddelniveau.
Viekira Pak er oftest, men ikke altid, samtidig administreret med ribavirin og behøver ikke tages med pegyleret interferon (peg-interferon).
Viekira Pak blev godkendt den 19. december 2014 af U.S. Food and Drug Administration (FDA) til anvendelse hos voksne 18 år eller derover med HCV genotypes 1 infektion, herunder dem med kompenseret cirrose (hvor leveren stadig fungerer) og levertransplantationer. For patienter med dekompenseret cirrose er Viekira Pak ikke anbefalet.
Viekira Pak er rapporteret at have en kur på 95% eller derover, hvor kun 2% af patienterne afslutter behandling på grund af intolerance. Det er hensigtsmæssigt til brug hos patienter med HIV / HCV-samtidig infektion.
Dosering
To tabletter af co-formulerede tabletter af ombitasvir + paritaprevir + ritonavir (25 mg / 150 mg / 100 mg) taget en dag om morgenen med mad plus en tabel med dasabuvir taget to gange dagligt om morgenen og aftenen med mad.
Tablettene leveres bekvemt sammen i daglige doseringsdoser, med doseringsinstruktioner, der følger med på hver æske. Den co-formulerede tablet er lyserød, filmovertrukket og præget med "AV1", mens dasabuvir tabletten er beige, filmcoated og præget med "AV2".
Prescribing Anbefalinger
Viekira Pak er ordineret i løbet af et 12- til 24-ugers forløb, ifølge følgende anbefalinger:
- Genotype 1a uden cirrhose: Viekira Pak med ribavirin i 12 uger
- Genotype 1a med cirrose: Viekira Pak med ribavirin i 24 uger
- Genotype 1b uden cirrhose: Viekira Pak alene i 12 uger
- Genotype 1b uden cirrhose: Viekira Pak med ribavirin i 24 uger
For levertransplantationspatienter kan Viekira Pak kun tages sammen med ribavirin i 24 uger, hvis leverfunktionen er normal og fibrose (ardannelse) er mindre.
Almindelige bivirkninger
De mest almindelige bivirkninger forbundet med brugen af Viekira Pak (forekommer hos op til 10% af patienterne) er:
- Træthed
- Kvalme
- Kløende hud
- Hudreaktioner
- Søvnløshed
- Svaghed og træthed
Lægemiddelinteraktioner
Den Følgende bør også undgås ved brug af Viekira Pak:
- Antikonvulsiver: carbamazepin, phenytoin, phenobarbital
- Antihyperlipidemika (bruges til at reducere lipidniveauer i blodet): gemfibrozil
- Anti-arytmi medicin: pimozid
- Cholesterolsænkende medicin: lovastatin, simvastatin
- Erektil dysfunktionsmedicin: Viagra (sildenafil)
- Ergotholdig medicin (bruges til behandling af hovedpine og migræne): ergotamin, dihydroergotamin, ergonovin, methylergonovin
- Ethinylestradiol (en menneskeskabt form af østrogen)
- HIV-medicin: Sustiva (efavirenz), Atripla (efavirenz + tenofovir + emtricitabin)
- Hypotension medicin: alfuzosin
- Rifampin-baserede anti-tuberkulosemedicin: Mycobutin, Rifater , Rifamat, Rimactane, Rifadin, Priftin
- Sedativer: Triazolam, Oralt Midazolam
Kontraindikationer og overvejelser
For patienter med moderat nedsat leverfunktion anbefales Viekira Pak ikke. Viekira Pak er kontraindiceret til patienter med svær nedsat leverfunktion.
Viekira Pak er også kontraindiceret til brug hos patienter med kendt hypersensivitet over for ritonavir (herunder Stevens-Johnsons syndrom, en potentielt livstruende inflammatorisk reaktion i hele kroppen).
Viekira Pak er kontraindiceret til brug hos gravide kvinder, når de anvendes sammen med ribavirin.
Det anbefales, at alle kvinder i den fødedygtige alder overvåges månedligt for graviditet i løbet af behandlingen. Det anbefales også, at patienten og hendes mandlige partner gives mindst to ikke-hormonelle præventionsmetoder, og at de anvendes i løbet af behandlingen og i seks måneder bagefter.